Усе про вуглеводні алкани, алкени та алкіни
Вуглеводні — це органічні сполуки, які складаються лише з атомів Карбону (C) і Гідрогену (H). Вони є основою органічної хімії, адже з них починається розуміння складніших речовин.
Серед усіх вуглеводнів особливо важливі три групи — алкани, алкени та алкіни. Вони відрізняються між собою типом зв’язків між атомами Карбону, і саме це визначає їхні властивості.
У цій статті ми розповімо вам про формули алканів, алкенів та алкінів, їхні хімічні властивості, відмінності та реакції.
Що таке алкани?
Алкани — це насичені вуглеводні, у яких між атомами Карбону є тільки одинарні зв’язки (—C—C—). Це найпростіший і найстабільніший клас органічних сполук.
Простіше кажучи, алкани — це «максимально насичені» молекули, де кожен атом Карбону зв’язаний із максимально можливою кількістю атомів Гідрогену.
Формули алканів
Загальна формула алканів: CnH2n+2
Це означає, що: якщо в молекулі n атомів Карбону — то Гідрогену буде 2n + 2.
Приклади:
CH₄ — метан;
C₂H₆ — етан;
C₃H₈ — пропан;
C₄H₁₀ — бутан.
З кожним новим атомом Карбону утворюється новий представник ряду — це називається гомологічний ряд.
Хімічні та фізичні властивості алканів
Алкани — досить спокійні та малоактивні, адже всі їхні зв’язки міцні.
Хімічні властивості:
горіння — основна реакція, за якої виділяється багато тепла;
реакції заміщення — атоми Гідрогену можуть замінюватися іншими елементами;
термічний розклад — розщеплення великих молекул на менші.
Фізичні властивості:
перші алкани (метан, етан) — гази;
середні — рідини;
великі — тверді речовини;
не розчиняються у воді;
добре горять.
Де застосовують алкани?
Алкани мають величезне практичне значення. Фактично, більшість енергетики базується саме на алканах:
паливо (природний газ, бензин, пропан-бутан);
сировина для хімічної промисловості;
виробництво пластмас;
мастильні матеріали;
парафін (свічки, косметика).
Що таке алкени?
Алкени — це ненасичені вуглеводні, які містять хоча б один подвійний зв’язок між атомами Карбону (C=C).
Саме цей подвійний зв’язок робить їх значно більш реакційно здатними, ніж алкани.
Формули алкенів
Загальна формула алкенів: CnH2n
Приклади:
C₂H₄ — етен (етилен);
C₃H₆ — пропен;
C₄H₈ — бутен.
Подвійний зв’язок — це, умовно, слабке місце молекули, де найчастіше відбуваються реакції.
Хімічні властивості алкенів
Алкени набагато активніші за алкани. Їхні основні реакції:
реакції приєднання (до подвійного зв’язку приєднуються інші атоми);
гідрування (приєднання водню);
галогенування (приєднання галогенів);
гідратація (приєднання води);
полімеризація;
молекули з’єднуються у довгі ланцюги — утворюються полімери (наприклад, з етену отримують поліетилен).
Де застосовують алкени?
Алкени — основа сучасної хімічної промисловості. Майже весь пластик навколо нас — це результат реакцій алкенів:
виробництво пластмас (поліетилен, поліпропілен);
синтез спиртів, кислот;
виробництво каучуків;
виготовлення пакувальних матеріалів.

Що таке алкіни?
Алкіни — це ненасичені вуглеводні, які мають потрійний зв’язок між атомами Карбону (C≡C).
Це ще більш «енергетично насичені» та реакційно активні сполуки.
Формули алкінів
Загальна формула алкінів: CnH2n–2
Приклади:
C₂H₂ — етин (ацетилен);
C₃H₄ — пропін;
C₄H₆ — бутин.
Хімічні властивості алкінів
Алкіни — дуже реакційно здатні через потрійний зв’язок. Основні реакції:
реакції приєднання (подібні до алкенів, але інтенсивніші);
приєднання водню;
приєднання галогенів;
приєднання води;
горіння (горять дуже яскравим полум’ям);
полімеризація (у деяких випадках).
Де застосовують алкіни?
Найвідоміший представник — ацетилен. Його використовують для газового зварювання та різання металів, у хімічному синтезі, для виробництва пластмас і розчинників, а також — у лабораторіях. Ацетиленове полум’я дуже гаряче, тому воно ідеально підходить для обробки металів.
Гомологічний ряд: алкани, алкени, алкіни
Гомологічний ряд — це послідовність органічних сполук, у якій кожна наступна речовина відрізняється від попередньої на одну групу —CH₂—.
Для алканів:
метан CH₄;
етан C₂H₆;
пропан C₃H₈;
бутан C₄H₁₀.
Кожен наступний має +CH₂.
Для алкенів:
етен C₂H₄;
пропен C₃H₆;
бутен C₄H₈.
Для алкінів:
етин C₂H₂;
пропін C₃H₄;
бутин C₄H₆.
У межах одного гомологічного ряду речовини мають подібні хімічні властивості. Але фізичні властивості (температура кипіння, агрегатний стан) поступово змінюються.
Алкани, алкени, алкіни: приклади
Щоб не плутатися, зручно порівнювати ці три класи одночасно:
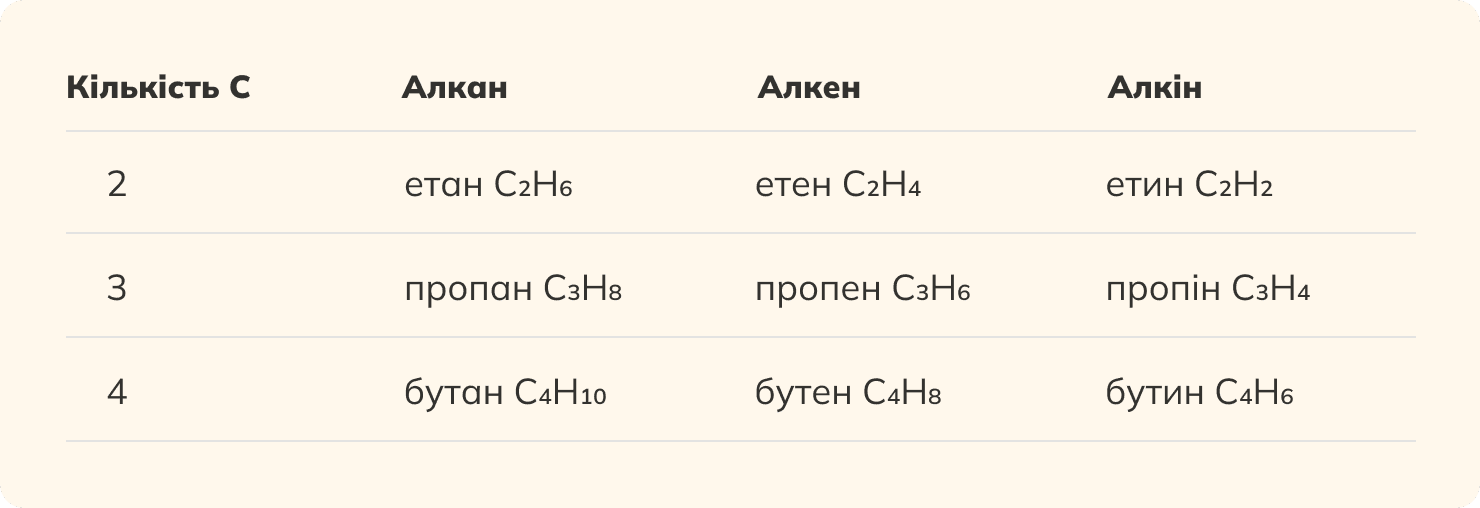
Головна різниця:
алкани мають тільки одинарні зв’язки;
алкени — один подвійний;
алкіни — один потрійний.
Через це алкани — найменш активні, а алкени й алкіни — значно реакційніші.
Поширені запитання
1. До якого класу вуглеводнів відносяться алкани?
Алкани належать до насичених вуглеводнів, тому що між атомами Карбону є лише одинарні зв’язки, а всі можливі зв’язки «заповнені» атомами Гідрогену.
2. З чим взаємодіють алкани?
Алкани малоактивні, але можуть реагувати з киснем (реакція горіння) та галогенами (реакції заміщення, наприклад із хлором). Більшість інших речовин із ними не реагує без спеціальних умов (світло, нагрівання).
3. З яким із галогенів алкани не взаємодіють?
Алкани практично не реагують із фтором у контрольованих умовах, бо реакція відбувається надто бурхливо й некеровано. Також дуже слабка взаємодія спостерігається з йодом.
4. Чи розчиняються алкани у воді?
Ні, алкани не розчиняються у воді. Причина проста: вода — полярна речовина, а алкани — неполярні. Зате вони добре розчиняються в органічних розчинниках.
5. З якою речовиною реагують алкени, алкіни та спирти?
Спільною реакцією для цих речовин є взаємодія з киснем (O₂) — усі вони можуть горіти. Також алкени й алкіни активно реагують із галогенами, а спирти — з активними металами та кислотами
6. Із яких природних сировин добувають алкани?
Основні джерела: природний газ, нафта і кам’яне вугілля (частково). Саме тому алкани є основою паливної енергетики.
7. Як алкани реагують з киснем?
Алкани горять, утворюючи вуглекислий газ (CO₂) та воду (H₂O), і виділяють багато тепла Якщо кисню недостатньо — може утворюватися чадний газ (CO) або сажа.
8. Які алкани є газами?
Перші представники гомологічного ряду: метан (CH₄), етан (C₂H₆), пропан (C₃H₈), бутан (C₄H₁₀).
Отже, підсумовуємо:
Алкани — стабільні й використовуються як паливо.
Алкени — активні та лежать в основі виробництва пластмас.
Алкіни — ще реакційніші й застосовуються в техніці та синтезі.
Ця тема стане значно зрозумілішою, якщо її розібрати на прикладах і задачах з репетитором хімії. Головне — практика, завдяки якій ви зможете використовувати ці формули автоматично.
Для ефективної підготовки до НМТ з хімії додаткові заняття з викладачем необхідні, щоб закріпити весь матеріал в індивідуальному форматі.
 Ознайомтеся з нашими послугами
Ознайомтеся з нашими послугами